فهرست مطالب این مقاله:
1. توسعه اسیدهای آمینه
2. خصوصیات ساختاری
3 ترکیب شیمیایی
4. طبقه بندی
5. سنتز
6. خصوصیات فیزیکوشیمیایی
7. سمیت
8 فعالیت ضد میکروبی
9. خصوصیات رئولوژیکی
10. برنامه های کاربردی در صنعت آرایشی
11. برنامه های کاربردی در لوازم آرایشی روزمره
سورفاکتانتهای اسید آمینه (AAS)یک کلاس از سورفاکتانت ها هستند که با ترکیب گروه های آبگریز با یک یا چند اسید آمینه تشکیل می شوند. در این حالت ، اسیدهای آمینه می توانند مصنوعی یا از هیدرولیزهای پروتئین یا منابع تجدید پذیر مشابه حاصل شوند. در این مقاله جزئیات بیشتر مسیرهای مصنوعی موجود برای AAS و تأثیر مسیرهای مختلف بر خصوصیات فیزیکوشیمیایی محصولات نهایی از جمله حلالیت ، پایداری پراکندگی ، سمیت و تجزیه و تحلیل پذیری قرار دارد. به عنوان یک کلاس از سورفاکتانت ها در افزایش تقاضا ، تطبیق پذیری AA به دلیل ساختار متغیر آنها تعداد زیادی فرصت تجاری را ارائه می دهد.
با توجه به اینکه سورفاکتانت ها به طور گسترده در مواد شوینده ، امولسیون کننده ها ، مهار کننده های خوردگی ، بازیابی روغن سوم و داروهای دارویی مورد استفاده قرار می گیرند ، محققان هرگز از توجه به سورفاکتانت ها خودداری نکرده اند.
سورفاکتانت ها نماینده ترین محصولات شیمیایی هستند که به طور روزانه در مقادیر زیادی در سراسر جهان مصرف می شوند و تأثیر منفی بر محیط آبزیان داشته اند.مطالعات نشان داده اند که استفاده گسترده از سورفاکتانتهای سنتی می تواند تأثیر منفی بر محیط زیست داشته باشد.
امروزه ، سمیت غیر سمی ، تجزیه پذیری و زیست سازگاری تقریباً به همان اندازه ابزار و عملکرد سورفاکتانت ها برای مصرف کنندگان مهم است.
بیوسورفاکتانتها سورفاکتانتهای پایدار سازگار با محیط زیست هستند که به طور طبیعی توسط میکروارگانیسم هایی مانند باکتری ها ، قارچ ها و مخمرها یا به صورت خارج سلولی ترشح می شوند.بنابراین ، بیوسورفاکتانتها همچنین می توانند با طراحی مولکولی برای تقلید از ساختارهای آمفیفیلیک طبیعی ، مانند فسفولیپیدها ، گلیکوزیدهای آلکیل و اسیدهای آمینه اسیل تهیه شوند.
سورفاکتانتهای اسید آمینه (AAS)یکی از سورفاکتانت های معمولی است که معمولاً از مواد اولیه حیوانی یا کشاورزی حاصل می شود. در طی دو دهه گذشته ، AA ها به عنوان سورفاکتانت های جدید مورد توجه دانشمندان را به خود جلب کرده اند ، نه تنها به این دلیل که می توان آنها را از منابع تجدید پذیر سنتز کرد ، بلکه به این دلیل که AA ها به راحتی قابل تجزیه هستند و دارای محصولات جانبی بی ضرر هستند و آنها را برای محیط زیست ایمن تر می کند.
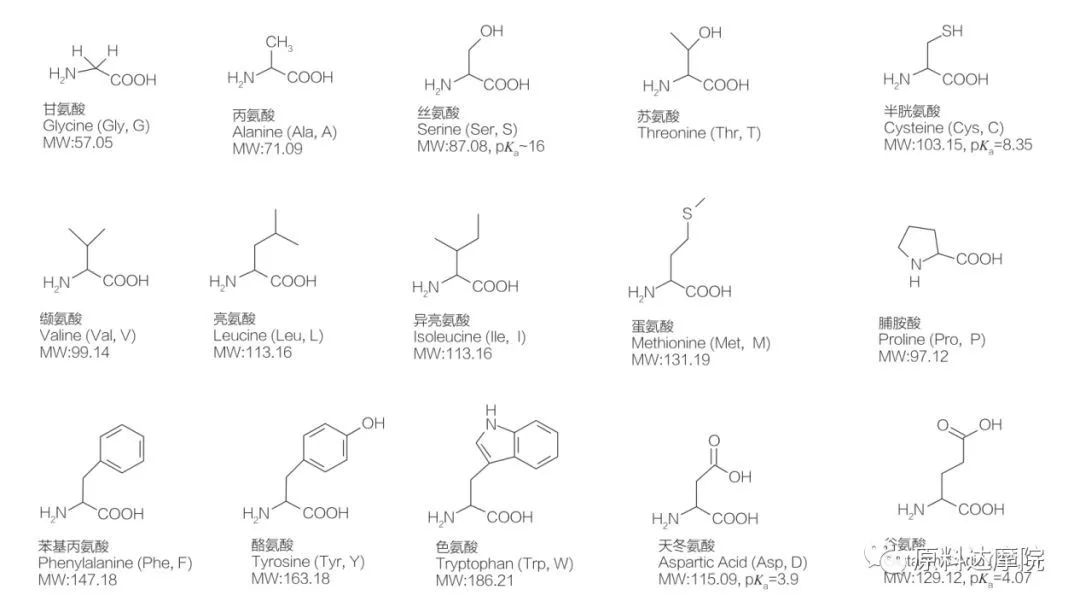
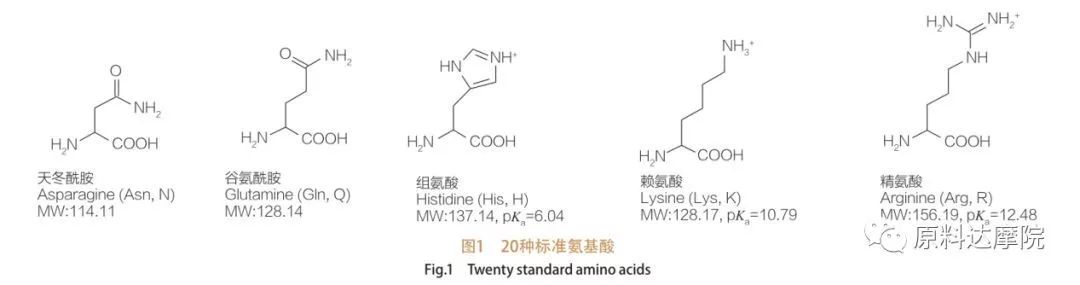
AA ها را می توان به عنوان یک کلاس از سورفاکتانت ها متشکل از اسیدهای آمینه حاوی گروه های آمینه اسید (HO 2 C-CHR-NH 2) یا باقیمانده اسید آمینه تعریف کرد (HO 2 C-CHR-NH-). 2 منطقه عملکردی اسیدهای آمینه باعث مشتق طیف گسترده ای از سورفاکتانت ها می شوند. در مجموع 20 اسید آمینه پروتئیژنیک استاندارد در طبیعت وجود دارد و مسئول تمام واکنشهای فیزیولوژیکی در رشد و فعالیت های زندگی است. آنها فقط با توجه به باقیمانده R از یکدیگر متفاوت هستند (شکل 1 ، PK A لگاریتم منفی ثابت تفکیک اسید محلول است). برخی از آنها غیر قطبی و آبگریز هستند ، برخی قطبی و آبگریز ، برخی اساسی و برخی اسیدی هستند.
از آنجا که اسیدهای آمینه ترکیبات تجدید پذیر هستند ، سورفاکتانتها که از اسیدهای آمینه سنتز می شوند نیز از پتانسیل بالایی برای پایدار و سازگار با محیط زیست برخوردار هستند. ساختار ساده و طبیعی ، سمیت کم و تجزیه پذیری سریع اغلب آنها را نسبت به سورفاکتانتهای معمولی برتر می کند. با استفاده از مواد اولیه تجدید پذیر (به عنوان مثال اسیدهای آمینه و روغنهای گیاهی) ، AA ها می توانند توسط مسیرهای مختلف بیوتکنولوژیکی و مسیرهای شیمیایی تولید شوند.
در اوایل قرن بیستم ، اسیدهای آمینه برای اولین بار به عنوان بستر برای سنتز سورفاکتانت ها مورد استفاده قرار گرفتند.AA ها عمدتاً به عنوان مواد نگهدارنده در فرمولاسیون دارویی و زیبایی مورد استفاده قرار می گرفتند.علاوه بر این ، AA ها از نظر بیولوژیکی در برابر انواع باکتری ها ، تومورها و ویروس های ایجاد کننده بیماری فعال بودند. در سال 1988 ، در دسترس بودن AA های کم هزینه باعث ایجاد علاقه تحقیق به فعالیت های سطحی شد. امروزه با توسعه بیوتکنولوژی ، برخی از اسیدهای آمینه نیز قادر به سنتز تجاری در مقیاس بزرگ توسط مخمر هستند ، که به طور غیرمستقیم ثابت می کند که تولید AAS سازگار با محیط زیست است.
01 توسعه اسیدهای آمینه
در اوایل قرن نوزدهم ، هنگامی که برای اولین بار اسیدهای آمینه به طور طبیعی کشف شد ، ساختارهای آنها بسیار با ارزش پیش بینی می شد - به عنوان مواد اولیه برای تهیه آمفیفیل ها قابل استفاده است. اولین مطالعه در مورد سنتز AAS توسط Bondi در سال 1909 گزارش شد.
در این مطالعه ، N-Asylglycine و N-Asylalanine به عنوان گروه های آبگریز برای سورفاکتانت ها معرفی شدند. کار بعدی شامل سنتز اسیدهای لیپوماینو (AAS) با استفاده از گلیسین و آلانین و هنتریچ و همکاران بود. مجموعه ای از یافته ها را منتشر کرد ،از جمله اولین کاربرد ثبت اختراع ، در مورد استفاده از نمک های آکیل سارکوزینات و آسیل آسپارتات به عنوان سورفاکتانت در محصولات تمیز کننده خانگی (به عنوان مثال شامپو ، مواد شوینده و خمیردندان).پس از آن ، بسیاری از محققان در مورد سنتز و خصوصیات فیزیکوشیمیایی اسیدهای آمینه اسیل بررسی کردند. تا به امروز ، ادبیات زیادی در مورد سنتز ، خواص ، کاربردهای صنعتی و تجزیه پذیری AAS منتشر شده است.
02 خاصیت ساختاری
زنجیره های اسید چرب آبگریز غیر قطبی AA ممکن است در ساختار ، طول زنجیره و تعداد متفاوت باشد.تنوع ساختاری و فعالیت سطح بالای AAS تنوع ترکیبی گسترده و خصوصیات فیزیکوشیمیایی و بیولوژیکی آنها را توضیح می دهد. گروه های سر AA از اسیدهای آمینه یا پپتیدها تشکیل شده اند. تفاوت در گروه های سر ، جذب ، تجمع و فعالیت بیولوژیکی این سورفاکتانت ها را تعیین می کند. گروههای عملکردی در گروه سر ، سپس نوع AAS ، از جمله کاتیونی ، آنیونی ، غیر یونی و آمفوتریک را تعیین می کنند. ترکیبی از اسیدهای آمینه آبگریز و بخش های زنجیره بلند آبگریز یک ساختار آمفیفیلیک را تشکیل می دهد که باعث می شود مولکول بسیار سطح فعال باشد. علاوه بر این ، وجود اتم های کربن نامتقارن در مولکول به تشکیل مولکول های کایرال کمک می کند.
03 ترکیب شیمیایی
تمام پپتیدها و پلی پپتیدها محصولات پلیمریزاسیون این اسیدهای α- آمینه تقریباً 20 α- پروتئینی هستند. تمام 20 اسید آمینه α حاوی یک گروه عملکردی اسید کربوکسیلیک (-COOH) و یک گروه عملکردی آمینه (-NH 2) هستند که هر دو به یک اتم α- کربن α- کربن یکسان متصل هستند. اسیدهای آمینه توسط گروههای مختلف R متصل به α-carbon (به جز لیسین ، جایی که گروه R هیدروژن است) با یکدیگر متفاوت هستند. گروه های R ممکن است در ساختار ، اندازه و بار (اسیدیته ، قلیایی) متفاوت باشند. این اختلافات همچنین حلالیت اسیدهای آمینه در آب را تعیین می کند.
اسیدهای آمینه کایرال هستند (به جز گلیسین) و از نظر طبیعت از نظر نوری فعال هستند زیرا چهار جایگزین مختلف دارند که به کربن آلفا مرتبط هستند. اسیدهای آمینه دو سازه ممکن دارند. آنها با وجود این واقعیت که تعداد L-Stereoisomers به طور قابل توجهی بیشتر است ، آنها تصاویر آینه ای غیر همپوشانی از یکدیگر هستند. گروه R موجود در برخی از اسیدهای آمینه (فنیل آلانین ، تیروزین و تریپتوفان) آریل است و منجر به حداکثر جذب اشعه ماوراء بنفش در 280 نانومتر می شود. α-COOH اسیدی و α-NH 2 در اسیدهای آمینه قادر به یونیزاسیون هستند و هر دو استریوزومرها ، هر کدام که باشند ، تعادل یونیزاسیون را نشان می دهند که در زیر نشان داده شده است.
r-cooh ↔r-coo-+ ساعت+
r-nh3+↔r-nh2+ ساعت+
همانطور که در تعادل یونیزاسیون بالا نشان داده شده است ، اسیدهای آمینه حداقل دو گروه اسیدی ضعیف دارند. با این حال ، گروه کربوکسیل در مقایسه با گروه آمینو پروتئین بسیار اسیدی است. pH 7.4 ، گروه کربوکسیل در حالی که گروه آمینه پروتئین می شود ، محروم می شود. اسیدهای آمینه با گروه های R غیر قابل تحمل در این pH از نظر الکتریکی خنثی هستند و Zwitterion را تشکیل می دهند.
طبقه بندی 04
AA ها را می توان با توجه به چهار معیار طبقه بندی کرد ، که به نوبه خود در زیر شرح داده شده است.
4.1 با توجه به مبدا
| با توجه به مبدا ، AA ها را می توان به 2 دسته به شرح زیر تقسیم کرد. strate رده طبیعی برخی از ترکیبات طبیعی که حاوی اسیدهای آمینه هستند نیز توانایی کاهش تنش سطح/سطحی را دارند و برخی حتی از اثربخشی گلیکولیپیدها نیز فراتر می روند. این AA ها همچنین به عنوان لیپوپپتیدها شناخته می شوند. لیپوپپتیدها ترکیبات با وزن مولکولی کم هستند که معمولاً توسط گونه های باسیلوس تولید می شوند.
چنین AA ها بیشتر به 3 زیر طبقه تقسیم می شوند:سورفاکتین ، Iturin و Fengycin.
|
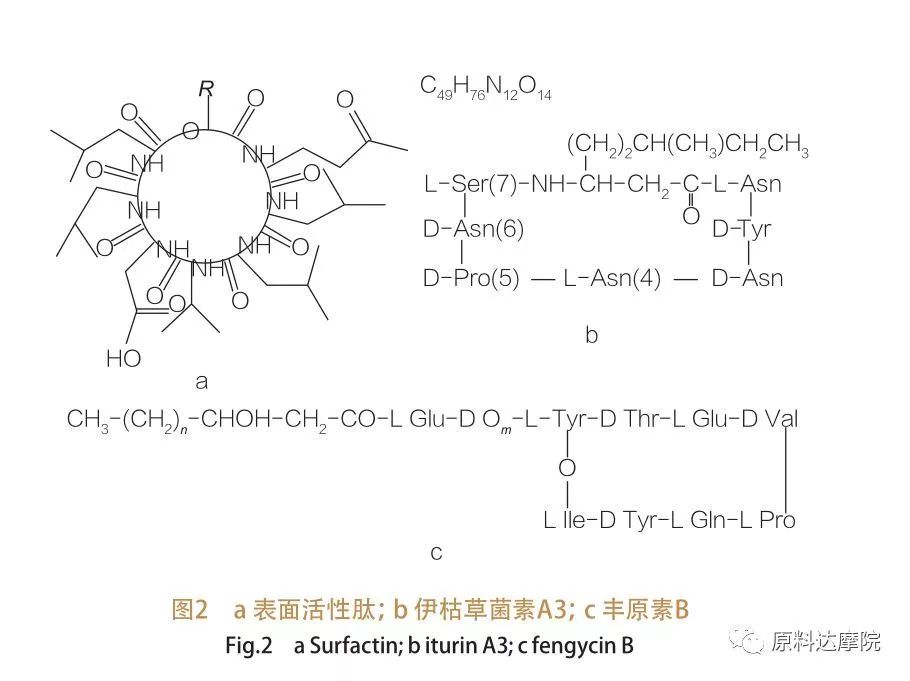
| خانواده پپتیدهای فعال سطح شامل انواع هپتپپتیدی انواع مواد ،همانطور که در شکل 2A نشان داده شده است ، که در آن یک زنجیره اسید چرب β- هیدروکسی غیر اشباع نشده اشباع شده با پپتید مرتبط است. پپتید فعال سطح یک لاکتون ماکروسیکلیک است که در آن حلقه با کاتالیز بین C- پایانه اسید چرب β- هیدروکسی و پپتید بسته می شود. در زیر کلاس Iturin ، شش نوع اصلی وجود دارد ، یعنی Iturin A و C ، Mycosubtilin و Bacillomycin D ، F و L.در همه موارد ، هپتپپتیدها با زنجیرهای C14-C17 اسیدهای چرب β-آمینه مرتبط هستند (زنجیرها می توانند متنوع باشند). در مورد ekurimycins ، گروه آمینه در موقعیت β می توانند پیوند آمید را با C- پایانه ایجاد کنند و در نتیجه یک ساختار لاکتام ماکروسیکلیک تشکیل می دهند.
زیر کلاس Fengycin حاوی Fengycin A و B است که وقتی Tyr9 Donfigured D- پیکربندی شده است ، به پلیپاستاتین نیز گفته می شود.دكاپپتید با زنجیره اسید چرب β -هیدروکسی اشباع شده یا اشباع نشده اشباع C14 -C18 مرتبط است. از لحاظ ساختاری ، پلیپاستاتین همچنین یک لاکتون ماکروسیکلیک است که حاوی یک زنجیره جانبی Tyr در موقعیت 3 از توالی پپتید و تشکیل پیوند استر با باقیمانده C- ترمینال است ، بنابراین یک ساختار حلقه داخلی تشکیل می دهد (مانند بسیاری از لیپوپپتیدهای سودوموناس).
strate رده مصنوعی AA ها همچنین می توانند با استفاده از هر یک از اسیدهای آمینه اسیدی ، اساسی و خنثی سنتز شوند. اسیدهای آمینه متداول مورد استفاده برای سنتز AA ها عبارتند از: اسید گلوتامیک ، سرین ، پرولین ، اسید آسپارتیک ، گلیسین ، آرژنین ، آلانین ، لوسین و هیدرولیزهای پروتئین. این زیر کلاس از سورفاکتانت ها را می توان با روش های شیمیایی ، آنزیمی و شیمی درمانی تهیه کرد. با این حال ، برای تولید AAS ، سنتز شیمیایی از نظر اقتصادی امکان پذیر است. نمونه های متداول شامل اسید N-lauroyl-l-glutamic و اسید N-palmitoyl-l-glutamic است.
|
4.2 بر اساس جایگزین های زنجیره ای آلیفاتیک
بر اساس جایگزین های زنجیره آلیفاتیک ، سورفاکتانتهای مبتنی بر اسید آمینه را می توان به 2 نوع تقسیم کرد.
با توجه به موقعیت جایگزین
| aa جایگزین AAS در ترکیبات جایگزین N ، یک گروه آمینه توسط یک گروه لیپوفیلی یا یک گروه کربوکسیل جایگزین می شود و در نتیجه باعث از بین رفتن پایه می شود. ساده ترین نمونه AA های N-جایگزین اسیدهای آمینه N-Asyl است که در اصل سورفاکتانت های آنیونی هستند. AA های جایگزین N دارای پیوند آمید هستند که بین قسمتهای آبگریز و آبگریز وصل شده است. پیوند آمید توانایی تشکیل پیوند هیدروژن را دارد ، که تخریب این سورفاکتانت را در یک محیط اسیدی تسهیل می کند ، بنابراین آن را تخریب پذیر می کند.
A AAS جایگزین در ترکیبات جایگزین C ، تعویض در گروه کربوکسیل (از طریق پیوند آمید یا استر) رخ می دهد. ترکیبات معمولی C جایگزین (به عنوان مثال استرها یا آمیدها) در اصل سورفاکتانتهای کاتیونی هستند.
AA- و C-جایگزین در این نوع سورفاکتانت ، هر دو گروه آمینه و کربوکسیل قسمت آبگریز هستند. این نوع در اصل یک سورفاکتانت آمفوتریک است. |
4.3 با توجه به تعداد دمهای آبگریز
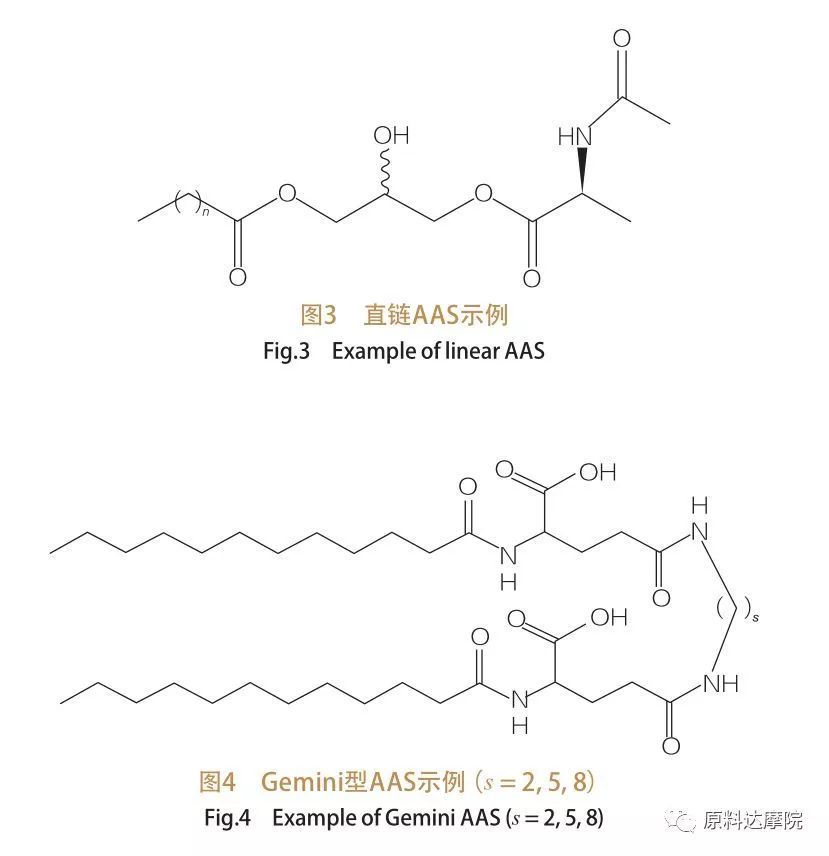
بر اساس تعداد گروههای سر و دم آبگریز ، AA ها را می توان به چهار گروه تقسیم کرد. AA های زنجیره ای مستقیم ، Gemini (Dimer) نوع AAS ، AA های Glycerolipid و AAS نوع آمفیفیلیک Bicephalic (BOLA). سورفاکتانت های زنجیره ای مستقیم سورفاکتانت هایی هستند که از اسیدهای آمینه با تنها یک دم آبگریز تشکیل شده اند (شکل 3). AA های نوع جمینی دارای دو گروه سر قطبی اسید آمینه و دو دم آبگریز در هر مولکول هستند (شکل 4). در این نوع ساختار ، دو AA های زنجیره ای مستقیم با یک فاصله به هم وصل می شوند و به همین دلیل به نام های دیمر نیز نامیده می شوند. در نوع AA های گلیسرولیپید ، از طرف دیگر ، دو دم آبگریز به همان گروه سر اسید آمینه وصل می شوند. این سورفاکتانت ها را می توان به عنوان آنالوگ های مونوگلیسیریدها ، دیسلیسیریدها و فسفولیپیدها در نظر گرفت ، در حالی که در AAS از نوع Bola ، دو گروه سر اسید آمینه توسط یک دم آبگریز مرتبط هستند.
4.4 با توجه به نوع گروه سر
aa ①Cationic AAS
گروه سر این نوع سورفاکتانت بار مثبت دارد. اولین AA های کاتیونی اتیل کوکیل آرگیل است که یک کربوکسیلات پیرولیدون است. خصوصیات منحصر به فرد و متنوع این سورفاکتانت باعث می شود که در ضد عفونی کننده ها ، عوامل ضد میکروبی ، عوامل ضد استاتیک ، تهویه مو و همچنین ملایم بودن روی چشم و پوست و به راحتی قابل تجزیه باشد. Singare و Mhatre AA های کاتیونی مبتنی بر آرژنین را سنتز کرده و خصوصیات فیزیکوشیمیایی آنها را ارزیابی کردند. در این مطالعه ، آنها ادعا کردند که بازده زیادی از محصولات به دست آمده با استفاده از شرایط واکنش Schotten-Baumann است. با افزایش طول زنجیره آلکیل و آبگریز ، فعالیت سطح سورفاکتانت افزایش می یابد و غلظت میسل بحرانی (CMC) کاهش می یابد. یکی دیگر از پروتئین های کواترنر آکیل است که معمولاً به عنوان تهویه مطبوع در محصولات مراقبت از مو استفاده می شود.
②ANIONIC AAS
در سورفکتانتهای آنیونی ، گروه سر قطبی سورفاکتانت بار منفی دارد. سارکوزین (CH 3 -NH -CH 2 -COOH ، N -METHYLGLYCINE) ، یک اسید آمینه که معمولاً در جوجه های دریایی و ستاره های دریایی یافت می شود ، از نظر شیمیایی با گلیسین (NH 2 -CH 2 -COOH) ، یک اسید آمینه اساسی که در سلول های پستانداران یافت می شود. -COOH ،) از نظر شیمیایی با گلیسین مرتبط است ، که یک اسید آمینه اساسی است که در سلولهای پستانداران یافت می شود. اسید لوریک ، اسید تترادکانوئیک ، اسید اولئیک و هالیدها و استرها معمولاً برای سنتز سورفکتانتهای سارکوزینات استفاده می شوند. سارکوزین ها ذاتاً خفیف هستند و بنابراین معمولاً در دهانشویه ، شامپو ، کف تراش اسپری ، ضد آفتاب ، پاک کننده های پوستی و سایر محصولات آرایشی مورد استفاده قرار می گیرند.
سایر AA های آنیونی در دسترس تجاری شامل Amisoft CS-22 و Amilitegck-12 است که به ترتیب نام تجاری سدیم N-Cocoyl-L-Glutamate و پتاسیم N-Cocoyl Glycinate هستند. آمیلیت معمولاً به عنوان ماده کف ، مواد شوینده ، محلول ، امولسیفایر و پراکندگی مورد استفاده قرار می گیرد و کاربردهای زیادی در لوازم آرایشی دارد ، مانند شامپو ، صابون حمام ، شستشوی بدن ، خمیردندان ، پاک کننده های صورت ، صابون های پاک کننده ، پاک کننده های لنزهای تماسی و سوخت های خانگی. Amisoft به عنوان پاک کننده پوستی و موهای خفیف ، عمدتاً در پاک کننده های صورت و بدن ، مواد شوینده مصنوعی ، محصولات مراقبت از بدن ، شامپو و سایر محصولات مراقبت از پوست استفاده می شود.
aa zwitterionic یا amphoteric
سورفاکتانتهای آمفوتریک حاوی هر دو سایت اسیدی و اساسی هستند و بنابراین می توانند با تغییر مقدار pH بار خود را تغییر دهند. در رسانه های قلیایی مانند سورفاکتانتهای آنیونی رفتار می کنند ، در حالی که در محیط های اسیدی مانند سورفکتانتهای کاتیونی و در رسانه های خنثی مانند سورفکتانتهای آمفوتریک رفتار می کنند. لوریل لیزین (LL) و آلکوکسی (2-هیدروکسی پروپیل) آرژنین تنها سورفاکتانت های آمفوتریک شناخته شده مبتنی بر اسیدهای آمینه هستند. LL یک محصول تراکم لیزین و اسید لوریک است. به دلیل ساختار آمفوتریک ، LL تقریباً در همه نوع حلالها نامحلول است ، به جز حلالهای بسیار قلیایی یا اسیدی. به عنوان یک پودر آلی ، LL چسبندگی بسیار خوبی به سطوح آبگریز و ضریب اصطکاک کم دارد و این توانایی روانکاری عالی را به این سورفکتانت می دهد. LL به طور گسترده در کرم های پوستی و نرم کننده مو استفاده می شود و همچنین به عنوان روان کننده استفاده می شود.
aa nonionic AAS
سورفاکتانتهای غیر یونی توسط گروههای قطبی بدون هزینه رسمی مشخص می شوند. هشت سورفاکتانت غیر یونی جدید اتوکسیله شده توسط الصباغ و همکاران تهیه شد. از اسیدهای α- آمینه محلول در روغن. در این فرآیند ، L- فنیل آلانین (LEP) و L- لوسین برای اولین بار با هگزادکانول استریز شدند و به دنبال آن با اسید پالمیتیک به دو آمید و دو استر اسید α- آمینه ارائه شد. آمیدها و استرها سپس با اتیلن اکسید واکنش تراکم با اتیلن اکسید برای تهیه سه مشتقات فنیل آلانین با تعداد متفاوتی از واحدهای پلیوکسی اتیلن (40 ، 60 و 100) تهیه کردند. این AA های غیر یونی که دارای مواد شوینده و خاصیت کف هستند ، یافت شد.
05 سنتز
5.1 مسیر مصنوعی اساسی
در AAS ، گروه های آبگریز می توانند به سایت های اسید آمین یا کربوکسیلیک یا از طریق زنجیره های جانبی اسیدهای آمینه وصل شوند. بر این اساس ، چهار مسیر مصنوعی اساسی ، همانطور که در شکل 5 نشان داده شده است ، موجود است.
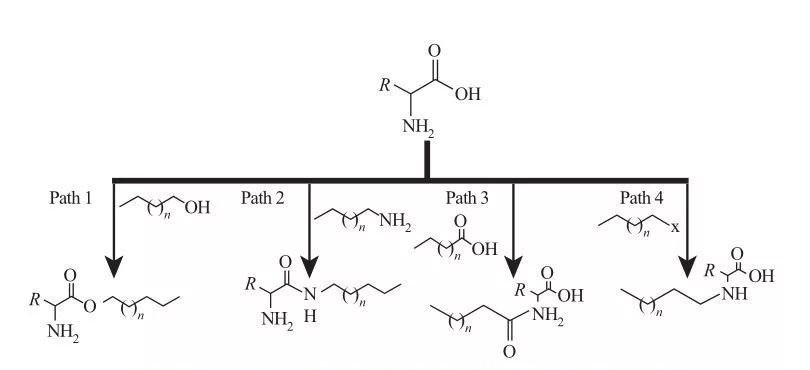
شکل 5 مسیرهای سنتز بنیادی سورفاکتانتهای مبتنی بر اسید آمینه
| مسیر 1. آمین های استر آمفیلیک با واکنش های استری سازی تولید می شوند ، در این صورت سنتز سورفاکتانت معمولاً با رفلکس الکل های چرب و اسیدهای آمینه در حضور یک ماده کم آب و یک کاتالیزور اسیدی حاصل می شود. در برخی از واکنش ها ، اسید سولفوریک هم به عنوان یک کاتالیزور و هم یک عامل کم آبی عمل می کند.
مسیر 2. اسیدهای آمینه فعال شده با آلکیل آمین ها واکنش نشان می دهند تا پیوندهای آمید تشکیل دهند ، و در نتیجه سنتز آمیدوامین های آمفیفیلیک ایجاد می شود.
مسیر 3. اسیدهای آمیدو با واکنش به گروههای آمین اسیدهای آمینه با اسیدهای آمیدو سنتز می شوند.
مسیر 4. اسیدهای آلکیل آمینه با زنجیره بلند با واکنش گروههای آمین با هالوکان ها سنتز شدند. |
5.2 پیشرفت در سنتز و تولید
5.2.1 سنتز اسید آمینه تک زنجیره ای/سورفاکتانتهای پپتید
اسیدهای آمینه N-Asyl یا O-Asyl یا پپتیدها را می توان با آسیلاسیون آنزیم کاتالیز شده گروههای آمین یا هیدروکسیل با اسیدهای چرب سنتز کرد. اولین گزارش در مورد سنتز کاتالیز شده لیپاز بدون حلال از اسید آمینه آمید یا مشتقات متیل استر که از کاندیدا قطب جنوب استفاده می شود ، با بازده بسته به اسید آمینه هدف از 25 ٪ تا 90 ٪. متیل اتیل کتون نیز در برخی از واکنش ها به عنوان یک حلال استفاده شده است. Vonderhagen و همکاران. همچنین واکنشهای N-actylation لیپاز و پروتئاز کاتالیز شده از اسیدهای آمینه ، هیدرولیزهای پروتئین و/یا مشتقات آنها را با استفاده از مخلوطی از آب و حلال های آلی (به عنوان مثال ، دی متیل فرمامید/آب) و متیل بوتیل کتون توصیف کرد.
در روزهای اولیه ، مشکل اصلی سنتز آنزیم کاتالیز شده AAS بازده کم بود. طبق Valivety و همکاران. عملکرد مشتقات اسید آمینه N-tetradecanoyl حتی 2 ٪ -10 ٪ حتی پس از استفاده از لیپازهای مختلف و انکوبه در 70 درجه سانتیگراد برای روزها بود. مونتت و همکاران. همچنین در مورد عملکرد کم اسیدهای آمینه در سنتز N-Asyl لیزین با استفاده از اسیدهای چرب و روغنهای گیاهی با مشکلات روبرو شده است. به گفته آنها ، حداکثر عملکرد محصول در شرایط عاری از حلال 19 ٪ و با استفاده از حلالهای آلی بود. همین مشکل توسط Valivety و همکاران روبرو شد. در سنتز مشتقات N-CBZ-L-lysine یا N-CBz-Lysine متیل استر.
در این مطالعه ، آنها ادعا كردند كه بازده 3-O-Tetradecanoyl-L-Serine 80 ٪ هنگام استفاده از سرین محافظت شده N به عنوان بستر و نووآوزیم 435 به عنوان یك كاتالیزور در محیط عاری از حلال مذاب. Nagao و Kito O-actialation of L-serine ، L-homoserine ، L-threonine و L-tyrosine (LET) را هنگام استفاده از لیپاز نشان داد ، نتایج واکنش (لیپاز توسط کاندیدا استوانه و ریزوپوس در محیط بافر کم آب به دست آمد) و گزارش داد که از نظر LAT-L-Homoserine از Acylerine acylerine استفاده می کند. Acylation of L-threonine و LeT رخ داده است.
بسیاری از محققان از استفاده از بسترهای ارزان قیمت و به راحتی در دسترس برای سنتز AA های مقرون به صرفه پشتیبانی کرده اند. سو و همکاران. ادعا کرد که تهیه سورفاکتانتهای مبتنی بر روغن نخل با لیپوآنزیم بی حرکت کار می کند. آنها خاطرنشان كردند كه با وجود واکنش وقت گیر (6 روز) ، بازده محصولات بهتر خواهد بود. Gerova و همکاران. سنتز و فعالیت سطحی از AA های کایرال N-palmitoyl بر اساس متیونین ، پرولین ، لوسین ، ترئونین ، فنیل آلانین و فنیل گلیسین در مخلوط چرخه ای/راسمیک بررسی شده است. PANG و CHU سنتز مونومرهای مبتنی بر اسید آمینه و مونومرهای مبتنی بر اسید دی کربوکسیلیک را در محلول توصیف کردند و یک سری از استرهای پلی آمید مبتنی بر اسید آمینه عملکردی و زیست تخریب پذیر با واکنشهای همبستگی در محلول سنتز شدند.
کانتوئوزن و گورریرو از استری شدن گروههای اسید کربوکسیلیک Boc-Ala-OH و Boc-Asp-OH با الکل های آلیفاتیک با زنجیره بلند و دیول ها ، با دیکلرومتان به عنوان حلال و آگارز 4B (Sepharose 4B) به عنوان کاتالیزور گزارش کردند. در این مطالعه ، واکنش Boc-Ala-OH با الکل های چرب تا 16 کربن بازده خوبی (51 ٪) داشت ، در حالی که برای کربن های BOC-ASP-OH 6 و 12 بهتر بود ، با عملکرد مربوط به 63 ٪ [64]. 99.9 ٪) در بازده از 58 ٪ تا 76 ٪ ، که با تشکیل پیوندهای آمید با آلکیل آمین های مختلف زنجیره ای طولانی یا پیوندهای استر با الکل های چرب توسط CBZ-ARG-OME سنتز شدند ، جایی که پاپاین به عنوان یک کاتالیزور عمل می کرد.
5.2.2 سنتز سورفاکتانتهای اسید آمینه/پپتید مبتنی بر جمینی
سورفاکتانتهای جمینی مبتنی بر اسید آمینه شامل دو مولکول AAS با زنجیره مستقیم است که توسط یک گروه فاصله دهنده سر به سر به یکدیگر متصل می شوند. 2 طرح ممکن برای سنتز شیمیایی سورفاکتانتهای مبتنی بر اسید آمینه از نوع جمینی وجود دارد (شکل 6 و 7). در شکل 6 ، 2 مشتق اسید آمینه با ترکیب به عنوان یک گروه فضا واکنش نشان می دهند و سپس 2 گروه آبگریز معرفی می شوند. در شکل 7 ، 2 ساختار زنجیره ای مستقیم به طور مستقیم توسط یک گروه فاصله دوقطبی به هم پیوند می خورند.
اولین توسعه سنتز آنزیم کاتالیز شده اسیدهای لیپوآمینو جمینی توسط Valivety و همکاران پیشگام شد. یوشیمورا و همکاران. سنتز ، جذب و تجمع یک سورفاکتانت جمینی مبتنی بر اسید آمینه بر اساس سیستین و برمید N-alkyl را مورد بررسی قرار داد. سورفاکتانتهای سنتز شده با سورفاکتانتهای مونومر مربوطه مقایسه شدند. فاوستینو و همکاران. سنتز AA های مونومریک مبتنی بر اوره آنیونی را بر اساس L-Cystine ، D-Cystine ، DL-Cystine ، L-Cysteine ، L-methionine و L-sulfoalanine و جفت های آنها با استفاده از وسیله هدایت ، تنش سطح تعادل و مشخصه فلوئورسانس پایدار از آنها توصیف کرد. نشان داده شد که با مقایسه مونومر و جمینی ، مقدار CMC جمینی کمتر بود.
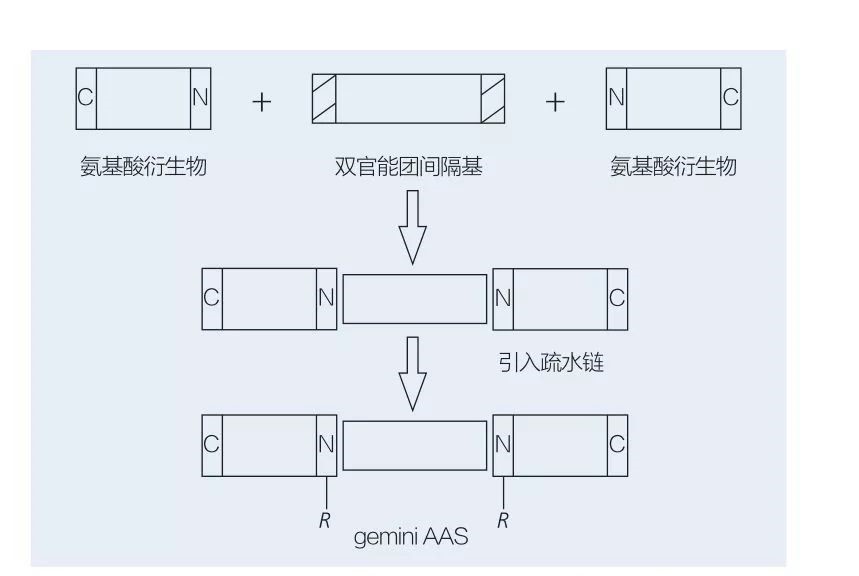
شکل 6 سنتز Gemini AAS با استفاده از مشتقات AA و فضا و به دنبال آن درج گروه آبگریز
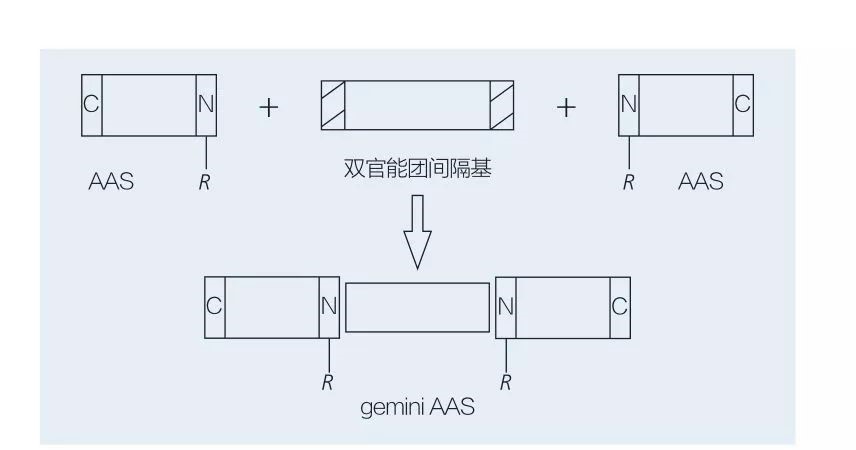
شکل 7 سنتز Gemini AAS با استفاده از فاصله دوتایی و AAS
5.2.3 سنتز آمینه گلیسرولیپید اسید/پپتید سورفاکتانتها
سورفاکتانت های آمینه گلیسرولیپید اسید/پپتید پپتید کلاس جدیدی از اسیدهای آمینه لیپید است که به دلیل ساختار یک یا دو زنجیره چرب با یک اسید آمینه مرتبط با یک پیوند استر ، به دلیل ساختار یک یا دو زنجیره چرب با یک یا دو زنجیره چرب که به یک یا دو زنجیره چرب متصل شده است ، به دلیل ساختار یک یا دو زنجیره چرب با یک یا دو زنجیره چرب همراه است. سنتز این سورفاکتانت ها با تهیه استرهای گلیسرول اسیدهای آمینه در دمای بالا و در حضور یک کاتالیزور اسیدی (به عنوان مثال BF 3) آغاز می شود. سنتز کاتالیز شده آنزیم (با استفاده از هیدرولازها ، پروتئازها و لیپازها به عنوان کاتالیزور) نیز گزینه خوبی است (شکل 8).
سنتز آنزیم کاتالیز شده از ترکیبات گلیسیریدهای آرژینین دلوئوریل شده با استفاده از پاپین گزارش شده است. سنتز ترکیبات استر دیاسیل گلیسرول از استیلارژینین و ارزیابی خصوصیات فیزیکوشیمیایی آنها نیز گزارش شده است.
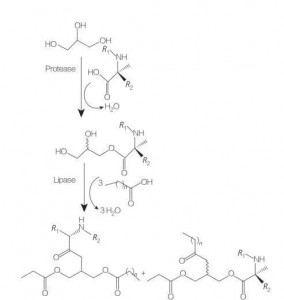
شکل 8 سنتز ترکیبات اسید آمینه مونو و دیاسیل گلیسرول
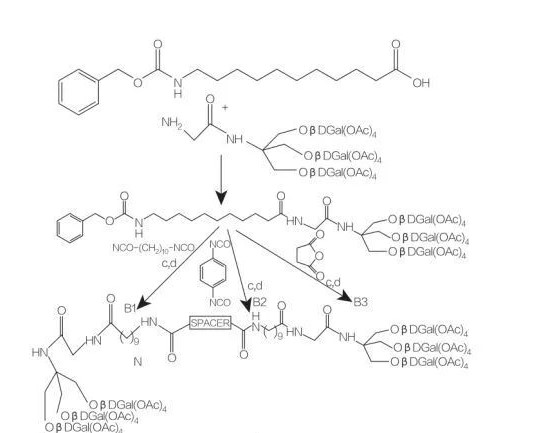
فاصله: NH- (CH2)10-NH: compoundb1
فاصله: NH-C6H4-NH: compoundb2
فاصله: Ch2-چ2: compoundb3
شکل 9 سنتز آمفیفیل های متقارن حاصل از تریس (هیدروکسی متیل) آمینومتان
5.2.4 سنتز سورفاکتانتهای اسید آمینه/پپتید مبتنی بر بولا
آمفایلهای نوع بلای مبتنی بر اسید آمینه حاوی 2 اسید آمینه هستند که به همان زنجیره آبگریز مرتبط هستند. Franceschi و همکاران. سنتز آمفیفیل های نوع Bola با 2 اسید آمینه (D- یا L-alanine یا L-histidine) و 1 زنجیره آلکیل با طول های مختلف را شرح داده و فعالیت سطح آنها را بررسی کرد. آنها در مورد سنتز و تجمع آمفیفیل های نوع جدید بولا با کسر اسید آمینه (با استفاده از اسید β آمینه غیر معمول یا الکل) و یک گروه فاصله C12 -C20 بحث می کنند. اسیدهای غیر آمینو غیر معمول مورد استفاده می توانند یک آمینو اسید قند ، اسید آمینه آزمونهای آزیدوتیمین (AZT) ، یک اسید آمینه نوربورن و یک الکل آمینه حاصل از AZT باشند (شکل 9). سنتز آمفیفیل های نوع متقارن بلای حاصل از تریس (هیدروکسی متیل) آمینومتان (TRIS) (شکل 9).
06 خواص فیزیکوشیمیایی
به خوبی شناخته شده است که سورفاکتانتهای مبتنی بر اسید آمینه (AAS) از نظر ماهیت متنوع و متنوع هستند و در بسیاری از کاربردها مانند حلالیت خوب ، خواص امولسیون خوب ، راندمان بالا ، عملکرد سطح بالا و مقاومت خوب در برابر آب سخت (تحمل یون کلسیم) کاربرد خوبی دارند.
بر اساس خواص سورفاکتانت اسیدهای آمینه (به عنوان مثال تنش سطح ، CMC ، رفتار فاز و دمای Krafft) ، نتیجه گیری زیر پس از مطالعات گسترده حاصل شد - فعالیت سطح AAS نسبت به همتای سورفکتانت معمولی آن برتر است.
6.1 غلظت میسل بحرانی (CMC)
غلظت میسل بحرانی یکی از پارامترهای مهم سورفاکتانت ها است و بسیاری از خصوصیات فعال سطح مانند حلالیت ، لیز سلولی و تعامل آن با بیوفیلم ها و غیره را حاکم می کند. به طور کلی ، افزایش طول زنجیره دم هیدروکربن (افزایش آبگریز) منجر به کاهش ارزش CMC محلول سوابق می شود و در نتیجه فعالیت سطح آن افزایش می یابد. سورفاکتانتهای مبتنی بر اسیدهای آمینه معمولاً در مقایسه با سورفاکتانتهای معمولی مقادیر CMC کمتری دارند.
از طریق ترکیب های مختلف گروه های سر و دم های آبگریز (آمید تک کاتیونی ، آمید دو کاتیونی ، استر مبتنی بر آمید دو کاتیونی) ، Infante و همکاران. سه AA مبتنی بر آرژنین را سنتز کرده و CMC و γCMC (تنش سطح در CMC) را مورد مطالعه قرار داده و نشان می دهد که مقادیر CMC و γCMC با افزایش طول دم آبگریز کاهش یافته است. در یک مطالعه دیگر ، Singare و Mhatre دریافتند که CMC سورفاکتانتهای N-α-Asylarginine با افزایش تعداد اتم های کربن دم آبگریز کاهش یافته است (جدول 1).
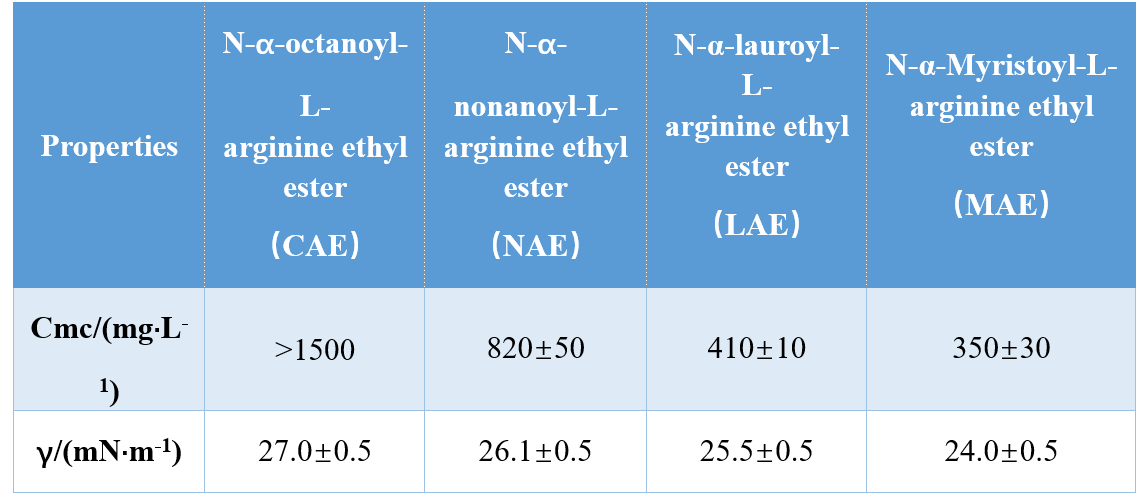
یوشیمورا و همکاران. CMC از سورفاکتانتهای جمینی مبتنی بر اسید آمینه مشتق از سیستئین را مورد بررسی قرار داد و نشان داد که CMC کاهش می یابد که طول زنجیره کربن در زنجیره آبگریز از 10 به 12 افزایش یابد. افزایش بیشتر طول زنجیره کربن به 14 منجر به افزایش CMC می شود ، که تأیید کرد که سوختگی های جمینی با زنجیره بلند گرایش کمتری به جمع دارند.
فاوستینو و همکاران. گزارش شکل گیری میسل های مخلوط در محلول های آبی سورفاکتانتهای جمینی آنیونی بر اساس سیستین. سورفاکتانتهای جمینی نیز با سورفکتانتهای مونومریک معمولی مربوطه (C 8 Cys) مقایسه شدند. مقادیر CMC مخلوط لیپید-سورفاکتانت پایین تر از مقادیر سورفاکتانتهای خالص است. سورفاکتانتهای جمینی و 1،2-diheptanoyl-sn-glyceryl-3-phosphocholine ، محلول در آب ، فسفولیپید تشکیل دهنده میسل ، در سطح میلی مولار CMC داشتند.
شرستا و آراماکی در مورد تشکیل میسل های کرم مانند ویسکوالاستیک در محلول های آبی سورفاکتانتهای آنیونی غیرونیک مبتنی بر اسید آمینه مخلوط در غیاب نمک های ترکیب بررسی کردند. در این مطالعه ، N-Dodecyl گلوتامات دمای Krafft بالاتری پیدا کرد. با این حال ، هنگامی که با اسید آمینه اصلی L-lysine خنثی شد ، میسل تولید کرد و محلول مانند یک مایع نیوتنی در 25 درجه سانتیگراد رفتار کرد.
6.2 حلالیت خوب آب
حلالیت خوب آب AA به دلیل وجود اوراق قرضه اضافی NH است. این امر باعث می شود AA ها تجزیه پذیر و سازگار با محیط زیست نسبت به سورفاکتانتهای معمولی مربوطه باشند. حلالیت آب N-Asyl-L- گلوتامیک اسید به دلیل 2 گروه کربوکسیل آن حتی بهتر است. حلالیت آب CN (CA) 2 نیز مناسب است زیرا 2 گروه آرژنین یونی در 1 مولکول وجود دارد که منجر به جذب و انتشار مؤثرتر در رابط سلولی و حتی مهار باکتریایی مؤثر در غلظت های پایین می شود.
6.3 دما کرفت و نقطه کرفت
دمای Krafft را می توان به عنوان رفتار حلالیت خاص سورفاکتانت ها که حلالیت آنها به شدت از دمای خاص افزایش می یابد ، درک کرد. سورفاکتانت های یونی تمایل به تولید هیدراتهای جامد دارند که می تواند از آب خارج شود. در دمای خاص (به اصطلاح دمای کرفت) ، افزایش چشمگیر و ناپیوسته در حلالیت سورفاکتانت ها مشاهده می شود. نقطه Krafft یک سورفاکتانت یونی دمای Krafft آن در CMC است.
این ویژگی حلالیت معمولاً برای سورفاکتانت های یونی مشاهده می شود و می تواند به شرح زیر توضیح داده شود: حلالیت مونومر رایگان سورفاکتانت در زیر دمای Krafft محدود است تا رسیدن به نقطه Krafft ، جایی که حلالیت آن به دلیل تشکیل میسل به تدریج افزایش می یابد. برای اطمینان از حلالیت کامل ، لازم است فرمولاسیون سورفاکتانت در دمای بالاتر از نقطه کرافت تهیه شود.
دمای Krafft از AAS مورد مطالعه قرار گرفته و با آن از سورفاکتانتهای مصنوعی معمولی مقایسه شده است. شراستا و آراماکی دمای Krafft AAS مبتنی بر آرژنین را مورد بررسی قرار دادند و دریافتند که غلظت میسل بحرانی رفتار تجمع را به شکل قبل از micells بالاتر از 2-5 × 10-6 mol-l-l-1 به نمایش می گذارد و پس از آن با استفاده از Sixize Sixy-Sixize Sixize (Oheta et al. رابطه بین دمای Krafft و باقیمانده اسید آمینه.
در این آزمایشات مشخص شد که دمای Krafft N-Hexadecanoyl AA با کاهش اندازه باقیمانده اسیدهای آمینه افزایش یافته است (فنیل آلانین یک استثناء است) ، در حالی که گرمای حلالیت (جذب حرارت) با کاهش اندازه باقیمانده اسیدهای آمینه (به استثنای گلیسین و فنلانین) افزایش یافته است. نتیجه گیری شد که در هر دو سیستم آلانین و فنیل آلانین ، تعامل DL از تعامل LL در شکل جامد نمک N-Hexadecanoyl AAS قوی تر است.
بریتو و همکاران. دمای KRAFFT سه سری از سورفاکتانتهای مبتنی بر اسید آمینه جدید را با استفاده از ریزگردها اسکن دیفرانسیل تعیین کرد و دریافت که تغییر یون trifluoroacetate به یون یدید منجر به افزایش قابل توجهی در دمای Krafft (حدود 6 درجه سانتیگراد) ، از 47 درجه سانتیگراد به 53 درجه سانتیگراد شد. حضور اوراق قرضه Cis-double و اشباع موجود در سرپرستان با زنجیره طولانی منجر به کاهش قابل توجهی در دمای Krafft شد. گزارش شده است که N-Dodecyl گلوتامات دارای دمای Krafft بالاتری است. با این حال ، خنثی سازی با اسید آمینه اصلی L- لیزین منجر به تشکیل میسل در محلول شد که مانند مایعات نیوتنی در 25 درجه سانتیگراد رفتار می کرد.
6.4 تنش سطح
تنش سطح سورفاکتانت ها به طول زنجیره قسمت آبگریز مربوط می شود. ژانگ و همکاران. تنش سطح گلیسینات سدیم کوکائیل را با روش صفحه Wilhelmy (0.2 25 25) درجه سانتیگراد تعیین کرد و مقدار تنش سطح را در CMC به عنوان 33 MN -M -1 ، CMC به عنوان 0.21 mmol -l -1 تعیین کرد. یوشیمورا و همکاران. تنش سطح 2C N Cys نوع تنش سطح بر اساس اسید آمینه را از عوامل فعال سطح 2C N مبتنی بر CYS تعیین کرد. مشخص شد که تنش سطح در CMC با افزایش طول زنجیره (تا 8 نفر) کاهش می یابد ، در حالی که روند برای سورفاکتانت ها با طول زنجیره ای n = 12 یا طولانی تر معکوس می شود.
تأثیر CAC1 2 بر تنش سطح سورفاکتانتهای مبتنی بر اسید آمینه دیکارکسیله شده نیز مورد بررسی قرار گرفته است. در این مطالعات ، CAC1 2 به محلول های آبی سه سورفاکتانت از نوع اسید آمینه دیکارکسیله شده اضافه شد (C12 Malna 2 ، C12 AspNA 2 و C12 Gluna 2). مقادیر فلات پس از CMC مقایسه شد و مشخص شد که تنش سطح در غلظت CAC1 2 بسیار کم کاهش می یابد. این به دلیل تأثیر یون های کلسیم بر ترتیب سورفاکتانت در رابط گاز گاز است. تنش های سطح نمک N-Dodecylaminomalonate و N-Dodecylaspartate ، از طرف دیگر ، تقریباً تا 10 میلی مول-L-1 CAC1 2 تقریباً ثابت بودند. بالاتر از 10 میلی مول -L -1 ، به دلیل تشکیل بارش نمک کلسیم سورفاکتانت ، تنش سطح به شدت افزایش می یابد. برای نمک دیودیوم N-Dodecyl گلوتامات ، افزودن متوسط CAC1 2 منجر به کاهش قابل توجهی در تنش سطح شد ، در حالی که ادامه افزایش در غلظت CAC1 2 دیگر باعث ایجاد تغییرات قابل توجهی نمی شود.
برای تعیین سینتیک جذب AA از نوع جمینی در رابط گاز گاز ، تنش سطح پویا با استفاده از روش حداکثر فشار حباب تعیین شد. نتایج نشان داد که برای طولانی ترین زمان آزمایش ، تنش سطح پویا 2C 12 Cys تغییر نمی کند. کاهش تنش سطح پویا فقط به غلظت ، طول دم آبگریز و تعداد دمهای آبگریز بستگی دارد. افزایش غلظت سورفاکتانت ، کاهش طول زنجیره و همچنین تعداد زنجیرها منجر به پوسیدگی سریعتر شد. نتایج به دست آمده برای غلظت بالاتر C Cys (8 تا 12 نفر) بسیار نزدیک به γ CMC اندازه گیری شده با روش Wilhelmy بود.
در یک مطالعه دیگر ، تنش های سطح دینامیکی سدیم دیستین سدیم (SDLC) و سدیم دیستیکامینو سیستین با روش صفحه Wilhelmy تعیین شد ، و علاوه بر این ، تنش های سطح تعادل محلول های آبی آنها با استفاده از روش حجم افت تعیین شد. واکنش اوراق دی سولفید نیز توسط سایر روشها نیز مورد بررسی قرار گرفت. علاوه بر این از mercaptoethanol به محلول 0.1 mmol -l -1sdlc منجر به افزایش سریع تنش سطح از 34 MN -M -1 به 53 MN -M -1 شد. از آنجا که NaClo می تواند پیوندهای دی سولفید SDLC را به گروههای اسید سولفونیک اکسیده شود ، هیچ مصالح مشاهده نشد که NaClo (5 mmol -L -1) به محلول 0.1 mmol -L -1 SDLC اضافه شد. میکروسکوپ الکترونی عبوری و نتایج پراکندگی نور پویا نشان داد که هیچ مصالح در محلول تشکیل نشده است. تنش سطح SDLC از 34 منگنز -1 -1 به 60 منگنز -متر در طی یک دوره 20 دقیقه افزایش یافته است.
6.5 تعامل سطح باینری
در علوم زندگی ، تعدادی از گروه ها خواص ارتعاشی مخلوط های AA های کاتیونی (دیاسییل گلیسرول آرژنین مبتنی بر آرژنین) و فسفولیپیدها را در رابط گاز گاز مورد مطالعه قرار داده اند ، سرانجام نتیجه می گیرند که این خاصیت غیر ایده آل باعث شیوع تعامل الکترواستاتیک می شود.
6.6 خاصیت تجمیع
پراکندگی نور پویا معمولاً برای تعیین خصوصیات تجمع مونومرهای مبتنی بر اسید آمینه و سورفاکتانتهای جمینی در غلظت های بالاتر از CMC استفاده می شود و به قطر هیدرودینامیکی ظاهری DH (= 2R ساعت) می رسد. مصالح تشکیل شده توسط C N Cys و 2Cn Cys نسبتاً بزرگ هستند و در مقایسه با سایر سورفاکتانت ها توزیع در مقیاس گسترده دارند. تمام سورفاکتانت ها به جز 2C 12 Cys به طور معمول سنگدانه های حدود 10 نانومتر را تشکیل می دهند. اندازه میسل سورفاکتانتهای جمینی به طور قابل توجهی بزرگتر از همتایان مونومر خود است. افزایش طول زنجیره هیدروکربن همچنین منجر به افزایش اندازه میسل می شود. اوتا و همکاران. خصوصیات تجمع سه استریوایزومر مختلف N-dodecyl-phenyl-alanyl-fenyl-fenyl-alanine در محلول آبی را شرح داده و نشان داد که دیاسترویزومرها غلظت تجمع بحرانی یکسانی در محلول آبی دارند. Iwahashi و همکاران. با استفاده از دیكروسم دایره ای ، NMR و فشار بخار اسمومتری شکل گیری سنگدانه های كیرال اسید N-Dodecanoyl-L-Glutamic ، N-Dodecanoyl-L-Valine و استرهای متیل آنها در حلالهای مختلف (مانند تتراهیدروفوران ، استونیتریل ، 1،4-دی هيسوره) مورد بررسی قرار گرفت. دوتایی ، NMR و اسمومتری فشار بخار.
6.7 جذب سطحی
جذب سطحی سورفاکتانتهای مبتنی بر اسید آمینه و مقایسه آن با همتای معمولی آن نیز یکی از مسیرهای تحقیق است. به عنوان مثال ، خصوصیات جذب سطحی استرهای دودسیل اسیدهای آمینه معطر به دست آمده از LET و LEP مورد بررسی قرار گرفت. نتایج نشان داد که LET و LEP به ترتیب مناطق بین سطحی کمتری در رابط گاز مایع و رابط آب/هگزان به ترتیب نشان داده اند.
بوردس و همکاران. رفتار محلول و جذب در رابط گاز گاز از سه سورفاکتانت اسید آمینه دی کربوکسیله شده ، نمکهای دیودیوم ددسیل گلوتامات ، دودسیل آسپارتات و آمینومالنات (با 3 ، 2 و 1 اتم کربن بین دو گروه کربوکسیل) را مورد بررسی قرار داد. براساس این گزارش ، CMC از سورفکتانتهای دیکارکسیله شده 4-5 برابر بیشتر از نمک گلیسین ددسیل ددسیل مونوکربوکسی شده بود. این امر به تشکیل پیوندهای هیدروژن بین سورفکتانتهای دیکارکسیله شده و مولکول های همسایه از طریق گروههای آمید در آن نسبت داده می شود.
6.8 رفتار فاز
مراحل مکعب ناپیوسته ایزوتروپیک برای سورفاکتانت ها در غلظت های بسیار بالا مشاهده می شود. مولکول های سورفاکتانت با گروه های سر بسیار بزرگ تمایل به تشکیل سنگدانه هایی از انحنای مثبت کوچکتر دارند. مارکز و همکاران. رفتار فاز سیستم های 12lys12/12Ser و 8lys8/16Ser (شکل 10 را ببینید) ، و نتایج نشان داد که سیستم 12lys12/12Ser) دارای یک منطقه جداسازی فاز بین مناطق محلول میکرولار و وزیکولار است ، در حالی که منطقه 8lys8/16Ser فازیکولیکیک 8lys8/16Ser سیستم کوچک و کوچک را نشان می دهد (Transuination Micenuration Smalllarated (Envoruination Small) لازم به ذکر است که برای منطقه وزیکول از سیستم 12lys12/12ser ، وزیکول ها همیشه با میسل همزیستی هستند ، در حالی که منطقه وزیکول سیستم 8lys8/16Ser فقط وزیکول دارد.
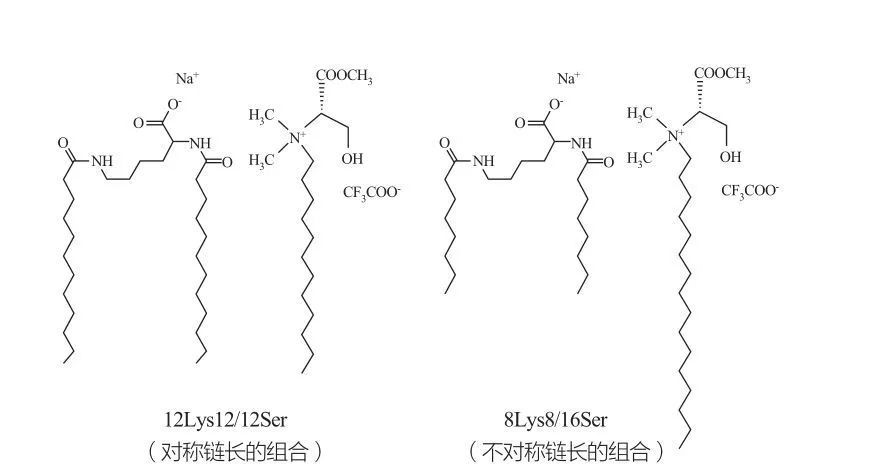
مخلوط های کاتانیونی از سورفاکتانتهای مبتنی بر لیزین و سرین: جفت متقارن 12lys12/12ser (سمت چپ) و جفت نامتقارن 8lys8/16Ser (راست)
6.9 توانایی امولسیون کننده
Kouchi و همکاران. توانایی امولسیون کننده ، تنش بین سطحی ، پراکندگی و ویسکوزیته N- [3-dodecyl-2-hydroxypropyl] -l-arginine ، l-glutamate و سایر AA ها را مورد بررسی قرار داد. در مقایسه با سورفاکتانتهای مصنوعی (همتایان غیر یونی و آمفوتریک معمولی آنها) ، نتایج نشان داد که AA ها توانایی امولسیون کننده قوی تری نسبت به سورفاکتانتهای معمولی دارند.
Baczko و همکاران. سورفاکتانتهای اسید آمینه آنیونی جدید سنتز شده و مناسب بودن آنها به عنوان حلال های طیف سنجی NMR با محوریت کایرال بررسی شده است. مجموعه ای از مشتقات آمفیفیلیک L-PHE یا L-ALA مبتنی بر سولفونات با دم های مختلف آبگریز (پنتیل ~ tetradecyl) با واکنش اسیدهای آمینه با انیدرید O-sulfobenzoic سنتز شدند. وو و همکاران. نمک های سدیم سنتز شده از Acyl AAS خستگی N وتوانایی امولسیون سازی آنها در امولسیون های روغن در آب را مورد بررسی قرار داد و نتایج نشان داد که این سورفاکتانت ها با اتیل استات به عنوان فاز روغن نسبت به N-Hexane به عنوان فاز روغن عملکرد بهتری دارند.
6.10 پیشرفت در سنتز و تولید
مقاومت در برابر آب سخت را می توان به عنوان توانایی سورفاکتانت ها در مقاومت در برابر حضور یونهایی مانند کلسیم و منیزیم در آب سخت ، یعنی توانایی جلوگیری از بارش در صابون های کلسیم درک کرد. سورفاکتانت ها با مقاومت در برابر آب سخت زیاد برای فرمولاسیون مواد شوینده و محصولات مراقبت شخصی بسیار مفید هستند. مقاومت در برابر آب سخت را می توان با محاسبه تغییر در حلالیت و فعالیت سطحی سورفاکتانت در حضور یونهای کلسیم ارزیابی کرد.
راه دیگر برای ارزیابی مقاومت در برابر آب سخت ، محاسبه درصد یا گرم سورفاکتانت مورد نیاز صابون کلسیم تشکیل شده از 100 گرم Oleate سدیم برای پراکندگی در آب است. در مناطقی با آب سخت زیاد ، غلظت بالای یون های کلسیم و منیزیم و محتوای مواد معدنی می تواند برخی کاربردهای عملی را دشوار کند. غالباً یون سدیم به عنوان ضد یون یک سورفاکتانت آنیونی مصنوعی استفاده می شود. از آنجا که یون کلسیم دو ظرفیتی به هر دو مولکول سورفاکتانت محدود می شود ، باعث می شود که سورفاکتانت با سرعت بیشتری از محلول را که بیشتر مواد شوینده را بیشتر می کند ، رسوب کند.
مطالعه مقاومت در برابر آب سخت AAS نشان داد که اسید و مقاومت در برابر آب سخت به شدت تحت تأثیر یک گروه کربوکسیل اضافی قرار گرفته است ، و با افزایش طول گروه فاصله بین دو گروه کربوکسیل ، اسید و مقاومت آب سخت بیشتر افزایش می یابد. ترتیب اسید و مقاومت در برابر آب سخت C 12 گلیسنات <C 12 آسپارتات <C 12 گلوتامات بود. به ترتیب با مقایسه پیوند آمید دیکاروکسیله شده و سورفکتانت آمینه دیکارکسیله شده ، مشخص شد که دامنه pH دومی گسترده تر است و با افزودن مقدار مناسب اسید ، فعالیت سطح آن افزایش یافته است. اسیدهای آمینه N-alkyl N-alkylated Dicarboxylated اثر کلات در حضور یونهای کلسیم را نشان داد و C 12 آسپارتات ژل سفید تشکیل داد. C 12 گلوتامات فعالیت سطح بالایی را در غلظت بالای Ca2 نشان داد و انتظار می رود در آب شیرین کن آب دریا استفاده شود.
6.11 پراکندگی
پراکندگی به توانایی یک سورفاکتانت در جلوگیری از همبستگی و رسوب سورفاکتانت در محلول اشاره دارد.پراکندگی ویژگی مهمی از سورفاکتانت ها است که باعث می شود آنها برای استفاده در مواد شوینده ، مواد آرایشی و دارویی مناسب باشند.یک ماده پراکندگی باید حاوی پیوند استر ، اتر ، آمید یا آمینه بین گروه آبگریز و گروه آبگریز ترمینال (یا در بین گروههای آبگریز زنجیره ای مستقیم) باشد.
به طور کلی ، سورفاکتانت های آنیونی مانند سولفات های آلکانولامیدو و سورفاکتانتهای آمفوتریک مانند آمیدوسولفوبتائین به ویژه به عنوان مواد پراکندگی صابون کلسیم مؤثر هستند.
بسیاری از تلاشهای تحقیقاتی ، پراکندگی AAS را تعیین کرده اند ، جایی که مشخص شد که N-Lauroyl Lysine با آب سازگار است و استفاده از آن برای فرمولاسیون های آرایشی دشوار است.در این سری ، اسیدهای آمینه اساسی N-Asyl جایگزین دارای پراکندگی فوق العاده ای هستند و در صنعت آرایشی برای بهبود فرمولاسیون استفاده می شوند.
07 سمیت
سورفاکتانتهای معمولی ، به ویژه سورفکتانتهای کاتیونی ، برای موجودات آبزی بسیار سمی هستند. سمیت حاد آنها به دلیل پدیده تعامل جذب-یون سورفاکتانتها در رابط سلول و آب است. کاهش CMC سورفاکتانت ها معمولاً منجر به جذب سطحی قوی تر سورفاکتانت ها می شود که معمولاً منجر به افزایش سمیت حاد آنها می شود. افزایش طول زنجیره آبگریز سورفاکتانت ها همچنین منجر به افزایش سمیت حاد سورفاکتانت می شود.بیشتر AA ها برای انسان و محیط زیست کم یا غیر سمی هستند (به ویژه برای موجودات دریایی) و برای استفاده به عنوان مواد غذایی ، داروهای دارویی و لوازم آرایشی مناسب هستند.بسیاری از محققان نشان داده اند که سورفاکتانتهای اسید آمینه ملایم و غیر تحریک کننده پوست هستند. سورفاکتانتهای مبتنی بر آرژنین نسبت به همتایان معمولی خود سمی کمتری دارند.
بریتو و همکاران. خواص فیزیکوشیمیایی و سم شناسی آمفیفیل های مبتنی بر اسید آمینه و [مشتقات آنها از تیروزین (Tyr) ، هیدروکسی پرولین (HYP) ، سرین (SER) و لیزین (لیز)] شکل خود به خودی وزیکولهای کاتیونی را مورد مطالعه قرار داد و داده هایی را در مورد سمیت حاد آنها به Daphnia Magna (IC 50) داده است. آنها وزیکولهای کاتیونی از dodecyltrimethylammonium Bromide (DTAB)/لیس- مشتقات و/یا مخلوط های سرخ/لیس- مشتق شده را سنتز کرده و آزمایش می کنند که اکوتوکسوسی و پتانسیل همولیتیک آنها را آزمایش می کند ، نشان می دهد که تمام AA ها و مخلوط های حاوی وزیکول آنها کمتر از سد سازی معمولی DTAB هستند.
روزا و همکاران. اتصال (ارتباط) DNA به وزیکولهای کاتیونی مبتنی بر اسید آمینه پایدار. بر خلاف سورفاکتانتهای کاتیونی معمولی ، که غالباً سمی به نظر می رسد ، به نظر می رسد تعامل سورفاکتانتهای اسید آمینه کاتیونی غیر سمی است. AA های کاتیونی مبتنی بر آرژنین است که به طور خودجوش وزیکول های پایدار را در ترکیب با برخی از سورفاکتانت های آنیونی تشکیل می دهد. مهارکننده های خوردگی مبتنی بر اسید آمینه نیز غیر سمی گزارش شده است. این سورفاکتانت ها به راحتی با خلوص بالا (حداکثر 99 ٪) ، کم هزینه ، به راحتی تخریب پذیر و کاملاً محلول در رسانه های آبی سنتز می شوند. مطالعات متعددی نشان داده اند که سورفاکتانتهای اسید آمینه حاوی گوگرد در مهار خوردگی برتر هستند.
در یک مطالعه جدید ، پرینلی و همکاران. مشخصات سم شناسی رضایت بخش از رامنولیپیدها در مقایسه با سورفاکتانتهای معمولی گزارش شده است. رامنولیپیدها به عنوان تقویت کننده نفوذپذیری عمل می کنند. آنها همچنین اثر رامنولیپیدها را بر نفوذپذیری اپیتلیال داروهای ماکرومولکولی گزارش دادند.
08 فعالیت ضد میکروبی
فعالیت ضد میکروبی سورفاکتانتها را می توان با حداقل غلظت مهاری ارزیابی کرد. فعالیت ضد میکروبی سورفاکتانتهای مبتنی بر آرژنین به تفصیل مورد بررسی قرار گرفته است. باکتری های گرم منفی نسبت به باکتری های گرم مثبت نسبت به سورفاکتانتهای مبتنی بر آرژنین مقاوم تر بودند. فعالیت ضد میکروبی سورفاکتانت ها معمولاً با حضور پیوندهای هیدروکسیل ، سیکلوپروپان یا اشباع نشده در زنجیره های آکیل افزایش می یابد. کاستیلو و همکاران. نشان داد که طول زنجیره های آکیل و بار مثبت مقدار HLB (تعادل آبگریز-لیپوفیلیک) مولکول را تعیین می کند ، و اینها در توانایی آنها در مختل کردن غشاها تأثیر دارند. Nα-Asylarginine Methyl Ester یکی دیگر از طبقه های مهم سورفاکتانتهای کاتیونی با فعالیت ضد میکروبی با طیف گسترده است و به راحتی زیست تخریب پذیر است و سمیت کم یا کمتری دارد. مطالعات در مورد تعامل Nα-Asylarginine متیل استر مبتنی بر سورفاکتانت با 1،2-dipalmitoyl-sn-propyltrioxyl-3-fosphorylcholine و 1،2-ditetradecanoyl-sn-fosphoryl-fosphorylcholine ، siveriers siveririers ، و با استفاده از ارگانیسم های زندگی در وجود Outrestranes Offection Of Outranes Of Outranss Offection Offeriroxylline ، و با استفاده از ارگانیک های خارجی ضد میکروبی نتایج نشان داد که سورفاکتانت ها فعالیت ضد باکتریایی خوبی دارند.
09 خصوصیات رئولوژیکی
خصوصیات رئولوژیکی سورفاکتانت ها نقش مهمی در تعیین و پیش بینی کاربردهای آنها در صنایع مختلف از جمله مواد غذایی ، داروسازی ، استخراج روغن ، مراقبت های شخصی و مراقبت از منزل دارند. بسیاری از مطالعات برای بحث در مورد رابطه بین ویسکوالاستیک اسید آمینه و CMC انجام شده است.
10 برنامه در صنعت آرایشی
AA در فرمولاسیون بسیاری از محصولات مراقبت شخصی استفاده می شود.گلیسینات پتاسیم N-Cocoyl بر روی پوست ملایم است و در پاکسازی صورت برای از بین بردن لجن و آرایش استفاده می شود. N-Asyl-L- گلوتامیک اسید دارای دو گروه کربوکسیل است که باعث می شود آب بیشتر محلول در آب باشد. در میان این AA ها ، AAS بر اساس اسیدهای چرب C 12 به طور گسترده ای در پاکسازی صورت برای از بین بردن لجن و آرایش استفاده می شود. AAS با زنجیره C 18 به عنوان امولسیفری در محصولات مراقبت از پوست استفاده می شود ، و نمک های آلانین n-lauryl شناخته می شوند که فوم های خامه ای ایجاد می کنند که برای پوست تحریک کننده نیست و بنابراین می تواند در فرمولاسیون محصولات مراقبت از کودک استفاده شود. AA های مبتنی بر N-lauryl که در خمیردندان استفاده می شود ، مواد شوینده خوبی شبیه به صابون و اثربخشی آنزیم قوی دارند.
طی چند دهه گذشته ، انتخاب سورفاکتانت ها برای مواد آرایشی ، محصولات مراقبت شخصی و داروهای دارویی بر روی سمیت کم ، خفیف ، لطافت نسبت به لمس و ایمنی متمرکز شده است. مصرف کنندگان این محصولات کاملاً از تحریک احتمالی ، سمیت و عوامل محیطی آگاه هستند.
امروزه از AA ها به دلیل مزایای فراوان در مورد همتایان سنتی خود در لوازم آرایشی و محصولات مراقبت شخصی ، برای تدوین بسیاری از شامپو ها ، رنگهای مو و صابون حمام استفاده می شود.سورفاکتانتهای مبتنی بر پروتئین دارای خواص مطلوب برای محصولات مراقبت شخصی هستند. برخی از AA ها دارای قابلیت های تشکیل فیلم هستند ، در حالی که برخی دیگر از قابلیت کف سازی خوبی برخوردار هستند.
اسیدهای آمینه به طور طبیعی عوامل مرطوب کننده در ذرت قشر وجود دارند. هنگامی که سلولهای اپیدرمی می میرند ، آنها بخشی از stratum corneum می شوند و پروتئین های داخل سلولی به تدریج به اسیدهای آمینه تخریب می شوند. این اسیدهای آمینه سپس بیشتر به داخل ذرت قشر منتقل می شوند ، جایی که آنها مواد چربی یا چربی مانند را به داخل ذرت قشر اپیدرمی جذب می کنند و از این طریق کشش سطح پوست را بهبود می بخشند. تقریباً 50 ٪ از فاکتور مرطوب کننده طبیعی در پوست از اسیدهای آمینه و پیرولیدون تشکیل شده است.
کلاژن ، یک ماده آرایشی رایج ، همچنین حاوی اسیدهای آمینه است که پوست را نرم نگه می دارد.مشکلات پوستی مانند زبری و کسل کننده تا حد زیادی به دلیل کمبود اسیدهای آمینه است. یک مطالعه نشان داد که مخلوط کردن یک اسید آمینه با پماد باعث سوزاندن پوست می شود و مناطق آسیب دیده بدون تبدیل شدن به زخم های کلوئیدی به حالت طبیعی خود بازگشتند.
اسیدهای آمینه نیز در مراقبت از کوتیکول های آسیب دیده بسیار مفید هستند.موهای خشک و بدون شکل ممکن است نشان دهنده کاهش غلظت اسیدهای آمینه در یک ذرت قشر به شدت آسیب دیده باشد. اسیدهای آمینه توانایی نفوذ در کوتیکول به داخل شافت مو را دارند و رطوبت را از پوست جذب می کنند.این توانایی سورفاکتانتهای مبتنی بر اسید آمینه باعث می شود که آنها در شامپو ، رنگ مو ، نرم کننده مو ، نرم کننده مو و وجود اسیدهای آمینه باعث تقویت موها شود.
11 برنامه در لوازم آرایشی روزمره
در حال حاضر ، تقاضای فزاینده ای برای فرمولاسیون مواد شوینده مبتنی بر اسید آمینه در سراسر جهان وجود دارد.AA شناخته شده است که از توانایی تمیز کردن بهتر ، توانایی کف سازی و خصوصیات نرم کننده پارچه برخوردار است و این باعث می شود آنها برای مواد شوینده خانگی ، شامپو ، شستشوی بدن و سایر کاربردهای مناسب باشند.گزارش شده است که AA های آمفوتریک مشتق از اسید آسپارتیک یک ماده شوینده بسیار مؤثر با خواص کلات هستند. استفاده از مواد مواد شوینده متشکل از اسیدهای N-alkyl-β-aminoethoxy برای کاهش سوزش پوست یافت شد. فرمولاسیون مواد شوینده مایع متشکل از N-cocoyl-β-aminopropionate گزارش شده است که یک ماده شوینده مؤثر برای لکه های روغن روی سطوح فلزی است. یک سورفاکتانت اسید آمینوکاربوکسیلیک ، C 14 Chohch 2 NHCH 2 COONA ، همچنین نشان داده شده است که از مواد شوینده بهتری برخوردار است و برای تمیز کردن منسوجات ، فرش ، مو ، شیشه و غیره استفاده می شود.
تهیه فرمولاسیون مواد شوینده مبتنی بر N- (N'-Long-Chain Acyl-β-alanyl) -β- آلانین توسط Keigo و Tatsuya در ثبت اختراع خود برای توانایی شستشوی بهتر و پایداری ، شکستن کف آسان و نرم شدن پارچه گزارش شده است. KAO فرمولاسیون مواد شوینده را بر اساس N-ACYL-1-N-HYDROXY-β-β- آلانین ایجاد کرده و از تحریک پوست کم ، مقاومت در برابر آب زیاد و قدرت برداشتن لکه بالا خبر داد.
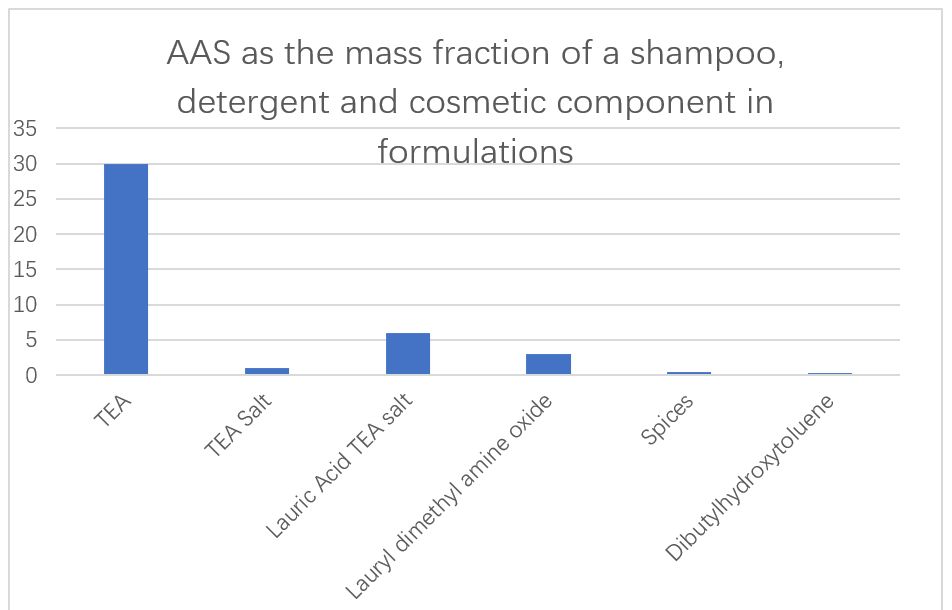
شرکت ژاپنی Ajinomoto از AA های کم سمی و به راحتی قابل تخریب بر اساس اسید L- گلوتامیک ، L-Arginine و L-lysine به عنوان مواد اصلی در شامپو ، مواد شوینده و مواد آرایشی استفاده می کند (شکل 13). توانایی مواد افزودنی آنزیم در فرمولاسیون مواد شوینده برای از بین بردن رسوب پروتئین نیز گزارش شده است. N-Asyl AAS حاصل از اسید گلوتامیک ، آلانین ، متیل گلیسین ، سرین و اسید آسپارتیک برای استفاده از آنها به عنوان مواد شوینده مایع عالی در محلول های آبی گزارش شده است. این سورفاکتانت ها حتی در دماهای بسیار کم ویسکوزیته را افزایش نمی دهند و می توان به راحتی از کشتی ذخیره سازی دستگاه کف سازی برای به دست آوردن کف همگن منتقل شد.
زمان پست: ژوئن -09-2022

